Xử lý khí thải Hydro Sunfua (H2S)
XỬ LÝ KHÍ THẢI HYDRO SUNFUA (H2S)
Xử lý khí thải Hydro Sunfua (H2S) – Công ty TNHH Đầu Tư Phát Triển TM XD Thiên Long
Khí thải Hydro sunfua H2S là vấn đề đã được đề cập đến trong nhiều công trình nghiên cứu, xử lý và tài liệu. Khí H2S là khí độc hại, không màu sắc nhưng có mùi khó chịu (mùi trứng thối) được đưa vào khí quyển với những lượng rất lớn có nguồn gốc tự nhiên và nhân tạo.
Khí H2S xuất hiện trong khí thải của các quá trình tinh chế dầu mỏ, tái sinh sợi hoặc khu vực chế biến thực phẩm, xử lý rác thải. Một phần H2S phát sinh trong tự nhiên bởi quá trình thối rữa của các chất hữu cơ dưới tác dụng của vi khuẩn từ rác thải, cống rãnh, bờ biển, ao tù, hồ nước cạn, kể cả từ các hầm lò khai thác than, các vệt núi lửa.
Vấn đề khí thải H2S thực sự trở thành vấn đề mang tính cấp bách và cần có những giải pháp hiệu quả nhằm kiểm soát và xử lý khí thải Hydro sunfua H2S triệt để tránh gây ảnh hưởng xấu đến sức khỏe và ô nhiễm môi trường.
Vấn đề phát thải khí H2S là một trong những vấn đề đang được quan tâm hiện nay không chỉ ở Việt Nam mà ở nhiều quốc gia trên thế giới. Để hiểu rõ hơn về khí H2S, cũng như là các công nghệ xử lý khí thải Hydro sunfua (H2S) thì dưới đây Thiên Long sẽ chia sẻ cho các bạn về cách xử lý khí thải Hydro sunfua (H2S) nhé!
1. Khái niệm về H2S
- Hydro sunfua (H2S) là một chất khí không màu, có mùi thối khó chịu (mùi trứng thối).
- Cấu trúc phân tử của H2S tương tự cấu trúc phân tử nước, H2S bị phân cực khả năng tạo thành liên kết Hydro ở H2S yếu hơn ở H2O.
- H2S ít tan trong nước nhưng lại tan nhiều trong dung môi hữu cơ. Các chất điện li không điện li trong H2S lỏng.
- H2S rất độc, nó độc không kém gì HCN. Ở trạng thái lỏng H2S bị oxy hóa một phần.
2. Nguồn gốc H2S
Hydro sunfua là loại khí chủ yếu tỏa ra trong quá trình luyện cốc từ than đá, quá trình lọc dầu, quá trình sản xuất khí công nghiệp. Hydro sunfua còn là một trong những thành phần của khí đốt thiên nhiên. Ngoài ra, trong một số ngành công nghiệp khác như chế biến xenlulozo, sợi nhân tạo, nấu bột giấy, thuộc da, nấu thuốc nhuộm, xử lý nước thải, lượng khí hydro sunfua tỏa ra cũng đáng kể.
Trước kia các hệ thống xử lý khí thải H2S và thu hồi khí H2S chủ yếu là phục vụ cho việc lọc sạch khí công nghiệp như khí đốt thiên nhiên.
Ngày nay các hệ thống này còn được phát triển mạnh cho nhu cầu giảm thiểu ô nhiễm bầu khí quyển, bảo vệ môi trường. Khí H2S thu hồi được từ các hệ thống xử lý có thể được biến đổi trực tiếp thành sản phẩm lưu huỳnh đơn chất hoặc khí SO2 để cung cấp nguyên liệu cho công đoạn sản xuất axit sunfuric nối tiếp theo.
3. Ảnh hưởng của khí H2S
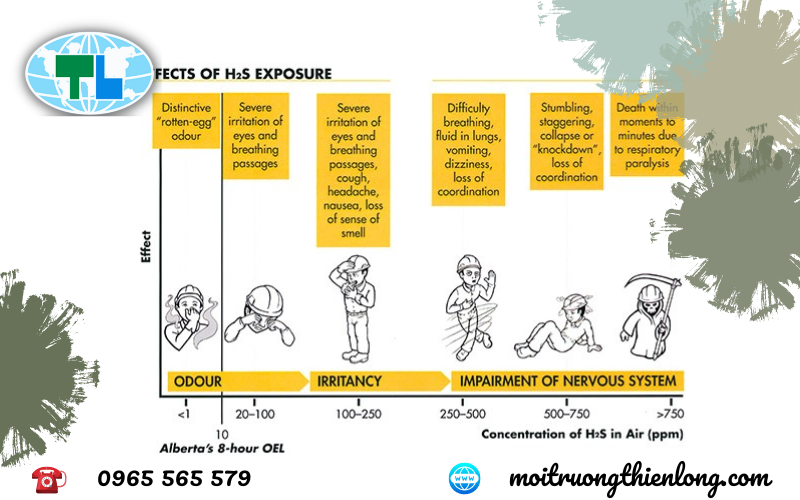
* Đối với con người
- Nồng độ 5 ppm gây ngộ độc, chóng mặt, nhức đầu.
- Nồng độ 500 ppm, gây viêm phổi và tiêu chảy.
- Nồng độ > 150 ppm, có thể gây tổn thương màng nhầy của cơ quan hô hấp, các triệu chứng có thể bao gồm đau đầu, buồn nôn, co giật, kích ứng mắt và da. Tổn thương hệ thần kinh trung ương có thể ngay lập tức và nghiêm trong sau khi tiếp xúc. Ở nồng độ cao, chỉ cần hít vài hơi là có thể bất tỉnh, hôn mê, liệt hô hấp, co giật, thậm chí tử vong.
- Tiếp xúc ngắn với H2S ở nồng độ từ 700 – 900ppm: chúng sẽ nhanh chóng xuyên qua màng túi phổi, xâm nhập vào mạch máu và gây tử vong. Ảnh hưởng đến phổi của việc tiếp xúc với khí H2S có thể không rõ ràng trong 72 giờ đầu sau khi đưa ra khỏi môi trường bị ảnh hưởng. Tuy nhiên, sau khi tiếp xúc với khí H2S ở nồng độ cao, sẽ dẫn đến hiện tượng phù phổi chậm, sự tích tụ chất lỏng dư thừa trong phổi cũng có thể xảy ra.
- Gây huyết áp thấp, nhức đầu, chán ăn, sụt cân: Khí H2S không tích tụ trong cơ thể, nhưng tiếp xúc nhiều có thể gây ra huyết áp thấp, nhức đầu, chán ăn và sụt cân. Tiếp xúc với nồng độ thấp trong thời gian dài có thể gây phát ban đau rát trên da và kích ứng mắt. Tiếp xúc nhiều lượng khí H2S cao có thể gây co giật, hôn mê, tổn thương não và tim, thậm chí tư vong.
Đối với các vật dụng kim loại
- Với tính chất nặng hơn không khí, khí H2S tích tụ ở những khu vực thấp của không gian thông gió kém. Khí H2S trong điều kiện không khí hơi ẩm có thể tạo thành axit sunfuric, có khả năng ăn mòn kim loại, giảm độ bền va đập của các thiết bị và dẫn đến hỏng hóc sớm.
– Dấu hiệu nhận biết bạn đã tiếp xúc với khí H2S
Trong trường hợp sau khi tiếp xúc với khí H2S, nhận thấy cơ thể có một số triệu chứng bất thường sau (thường xuất hiện trong 24 giờ):
- Ho, thở khò khè, khó thở, thở gấp
- Đau hoặc tức ngực
- Đau dạ dày, nôn mửa
- Đau đầu
- Tăng đỏ, đau hoặc chảy mủ từ vùng da bị bỏng
Hãy đảm bảo là bạn đã che chắn để bảo vệ đường hô hấp an toàn trước khi bước vào môi trường có khí H2S. Trong trường hợp xuất hiện một trong những triệu chứng ở trên bạn nên liên hệ ngay cho ngay bác sĩ hoặc đến cơ sở y tế để được chuẩn đoán và chữa trị kịp thời.
4. Xử lý khí thải Hydro sunfua (H2S) bằng phương pháp hấp thụ
4.1. Xử lý khí thải Hydro sunfua (H2S) bằng Natri cacbonat
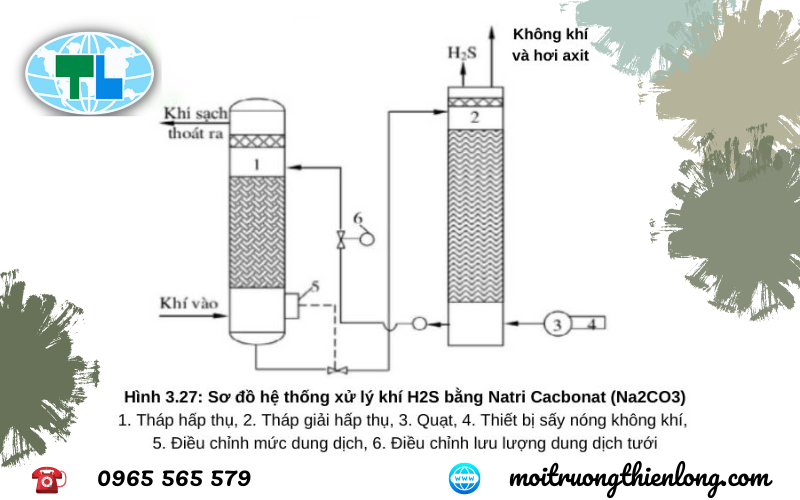
– Xử lý khí thải Hydro sunfua (H2S) bằng Natri cacbonat (Na2CO3)
- Quá trình xử lý khí thải H2S bằng Na2CO3 dựa trên cơ sở các phản ứng sau:
H2S + Na2CO3 = NaHS + NaHCO3
- Phản ứng thu hồi lưu huỳnh có sự tham gia của Natri vanadat NaVO3:
2NaHS + H2S + 4NaVO3 + 1/2O2 = Na2V4O9 + 4NaOH + 3S
- Để hoàn nguyên vanadat người ta dùng chất xúc tác ADA (natri-amoni vanadat và disunfonat):
Na2V4O9 + 2NaOH + 1/2O2 + 2ADA = 4NaVO3 + 2ADA
- Dễ dàng tuần hoàn và thu hồi hóa chất cho quá trình phản ứng => ít tốn hóa chất.
4.2. Xử lý khí thải Hydro sunfua bằng Kali photphat (K3PO4)
- Người ta có thể thay thế Na2CO3 bằng K3PO4
- Phản ứng khử H2S xảy ra như sau:
K2PO4 + H2S = K2HPO4 + KHS
– Ưu điểm:
- Có tính bền vững
- Dừng hơi nước để làm bay hơi và thu hồi H2S
- Phản ứng của nó với H2S mang tính chất chọn lựa khi có mặt của khí SO2 trong khí thải
- Ngoài ra, có thể dùng amoni cacbonat và kali cacbonat làm dung dịch hấp thụ đối với H2S:
(NH4)2CO3 + H2S = (NH4)2S + H2O + CO2
- Dung dịch (NH4)2S sau hấp thu được phân giải thành NH3 và H2S
(NH4)2S = NH3 và H2S
4.3. Xử lý khí thải Hydro sunfua (H2S) bằng xút (NaOH)
- Khí H2S kết hợp với NaOH theo các phản ứng sau đây:
H2S + 2NaOH = Na2S + 2H2O
Na2S + H2S = 2NaHS
Na2S + H2O = NaHS + NaOH
- Song song với các phản ứng trên, xút còn có tác dụng với cacbonic:
CO2 + NaOH = NaHCO3
NaHCO3 + NaOH = Na2CO3 + H2O
- Ngoài phản ứng khử H2S, trong dung dịch còn xảy ra quá trình oxy hóa natri sunfua Na2S thu được từ phản ứng ở trên (natri hydrosunfua và hyposunfit)
Na2S + H2O = NaHS + NaOH
2NaHS + 2O2 = Na2S2O3 + H2O
- Các phản ứng phụ trên là có lợi vì chúng góp phần làm giảm nhẹ khu xử lý dung dịch đã dùng xong trước khi thải ra hệ thống thoát nước.
- Ngoài dung dịch xút ra, chúng ta còn có thể dùng sữa vôi để thay thế. Lúc đó kết quả thu được của quá trình khử H2S, một cách tương tự như trường hợp dùng xút, là chất cặn nhão có chứa canxi sunfua (CaS) mà chất này cũng cần được xử lý trước khi thải ra ngoài.
- Dung dịch xút đã sử dụng cũng như chất bùn nhão thu được khi dùng sữa vôi thay thế có thể được xử lý bằng cách dùng vôi clorua hỗn hợp các chất Ca(ClO)2, CaCl2 và các Ca(OH)2 để oxy hóa các liên kết sunfit. Lượng vôi clorua dùng vào mục đích này là 6,3 kg quy về cho 1kg lưu huỳnh (với nồng độ clo trong vôi là 35%).
- Xử lý khí thải Hydro sunfua trong scrubo 1 với lớp đệm là khâu sứ Raschig. Hệ thống được thiết kế với một lượng dung dịch đã sử dụng được thải liên tục ra ngoài sau khi đã xử lý bằng vôi clorua. Nồng độ chất kiềm trong dung dịch hấp thụ đi vào scrubo được khống chế ở mức 7g/l.
- Vận tốc trong scrubo – 0,6 m/s. Lượng NaOH hoặc CaO tiêu hao quy về cho 1kg lưu huỳnh là 8kg. Phương pháp này đảm bảo khử được 100% H2S trong khí thải. Hệ thống xử lý khí thải Hydro sunfua không đòi hỏi chế tạo bằng vật liệu chống axit.
4.4. Xử lý khí thải Hydro sunfua bằng amoniac
Dùng amoniac để khử H2S trong khí thải là quá trình khá đơn giản và được áp dụng rộng rãi. Trong tháp hấp thụ, H2S trong khí thải tiếp xúc với dung dịch amoniac và chúng kết hợp với nhau theo phản ứng:
2NH3 + H2S = (NH4)2S
Ở nhiệt độ và áp suất thích hợp amoniac sunfua (NH4)2S phân giải thành NH3 và H2S. Amoniac quay lại chu trình làm việc, còn H2S được đưa sang công đoạn điều chế axit hoặc lưu huỳnh đơn chất.
4.5. Xử lý khí thải Hydro sunfua bằng dung dịch natri thioasenat (Na2As2S5O2)
Phản ứng hấp thụ khí H2S bằng dung dịch natri thioasenat xảy ra như sau:
H2S + Na2As2S5O2 = Na4As2S6O + H2O
Tiếp theo, natri thioasenat được hoàn nguyên theo phản ứng sau:
2Na4As2S6O + O2 = 2NaAs2S5O2 + 2S
Hai phản ứng nêu trên xảy ra rất nhanh và là các phản ứng chủ yếu trong hầu hết các điều kiện vận hành.
Trường hợp khi nồng độ ban đầu của H2S trong khí thải rất cao hoặc khi thời gian tiếp xúc giữa khí H2S và dung dịch hấp thụ kéo dài thì các phản ứng phụ, chậm hơn sau đây có thể xảy ra:
- Hấp thụ:
Na4As2S6O + H2S = Na4As2S7 + H2O
- Hoàn nguyên:
2Na4As2S7 + O2 = 2Na4As2S6O + 2S
Dung dịch hấp thụ natri thioasenat được chuẩn bị bằng cách hòa tan As2O3 và natri cacbonat (Na2CO3) trong nước với tỷ lệ: 1 mol As2O3; 2 mol Na2CO3. Trong dung dịch có: natri cacbonat và bicacbonat, natri asenit và axit asenic; các chất trên sẽ phản ứng xen kẽ với H2S và oxy để tạo thành natri thioasenat Na4As2S5O2.
Dung dịch bão hòa chảy ra từ đáy tháp hấp thụ 1 được bơm qua thiết bị cấp nhiệt 3 để hâm nóng đến nhiệt độ ≈ 45oC rồi đi vào tháp oxy hóa 4, trong đó dung dịch và không khí chuyển động cùng chiều từ dưới lên trên.
Không khí không những làm cho lưu huỳnh tách ra khỏi dung dịch mà còn có tác dụng như chất tạo bọt và lưu huỳnh dạng bọt sẽ nổi lên trên bề mặt của dạng dung dịch trong tháp oxy hóa rồi tràn qua vách ngăn trong thùng phân ly 5 để chảy vào thùng lắng 6. Dung dịch đã được hoàn nguyên từ thùng phân ly 5 tự chảy vào đỉnh tháp hấp thụ để tới cho lớp đệm rỗng trong tháp.
5. Xử lý khí thải Hydro sunfua (H2S) bằng phương pháp hấp phụ
5.1. Xử lý khí thải Hydro sunfua bằng chất hấp phụ Oxit sắt Fe2O3
Đây là phương pháp cổ điển nhất được dựa trên cơ sở các phản ứng sau:
Fe2O3 + 3H2S = Fe2S3 + 3H2O
2Fe2S3 + 3O2 = 2Fe2O3 + 6S
Sau khi bão hòa H2S, Oxit sắt được hoàn nguyên bằng không khí (cấp oxy) để thu lưu huỳnh. Tốc độ phản ứng hấp phụ H2S của oxit sắt phụ thuộc vào mức độ tiếp xúc giữa khí và bề mặt vật liệu hấp phụ. Do đó để nâng cao tốc độ phản ứng, độ rỗng (xốp) của vật liệu hấp phụ phải lớn. Thường độ rỗng của oxit sắt không nhỏ hơn 50%.
Điều kiện tốt nhất cho quá trình hấp phụ khí H2S bằng Oxit sắt là nhiệt độ nằm trong khoảng 28÷30oC và độ ẩm của vật liệu hấp phụ khoảng 30%.
Để hoàn nguyên có thể áp dụng các phương pháp khác nhau:
- Oxy hóa vật liệu hấp phụ bằng oxy trong không khí.
- Thổi hỗn hợp khí có chứa 2÷3% oxy qua lớp vật liệu hấp phụ. Nhiệt độ hoàn nguyên 600÷800oC.
- Hoàn nguyên liên tục khối vật liệu hấp phụ bằng cách bổ sung vào dòng khí cần xử lý một thể tích không khí với tính toán sao cho lượng oxy trong hỗn hợp khí gấn 1,5 lần lượng oxy lý thuyết cần cho quá trình oxy hóa. Như vật quá trình hoàn nguyên sẽ xảy ra song song với quá trình hấp phụ
5.2. Xử lý khí thải Hydro sunfua bằng than hoạt tính
Qúa trình xử lý khí thải Hydro sunfua (H2S) bằng than hoạt tính xảy ra nhờ hiện tượng oxy hóa khí H2S trên bề mặt của than theo phản ứng:
H2S + 1/2O2 = H2O + S + 222 kJ/mol
Để thúc đẩy quá trình oxy hóa thêm vào khí cần lọc một lượng nhỏ amoniac (0,2 g/m3).
Lưu huỳnh được giải phóng ra trong phản ứng oxy hóa nêu trên dần dần tích tụ trong lớp than và làm cho vật liệu hấp phụ trở nên bão hòa, lúc đó cần tiến hành hoàn nguyên vật liệu hấp phụ bằng amoni sunfua (NH4)2S theo phản ứng:
2(NH4)2S + 6S = 2(NH4)2S4
hoặc là:
(NH4)2S + (n-1)S = (NH4)2Sn
Sau đó dung dịch được phân hủy bằng hơi ở nhiệt độ 125÷130oC và áp suất ( 1,7/2).105 Pa để thu lại amoni sunfua (NH4)2S và lưu huỳnh đơn chất:
(NH4)2Sn = (NH4)2S + (n-1)S
Lưu huỳnh thu được có thể tách ra khỏi dung dịch nhờ sự khác nhau về khối lượng đơn vị. Độ tinh khiết của lưu huỳnh có thể đạt 99,9%, còn hơi ngưng tụ lại trong quá trình phân hủy dung dịch là amoni sunfua sạch.
Sau khi tách lưu huỳnh ra khỏi than bão hòa, người ta rửa than bằng nước cho tới khi không còn SO2 trong nước mới tôi, sau đó than được sấy khô để dùng trở lại.
Sơ đồ hệ thống xử lý khí thải Hydro sunfua (H2S) bằng than hoạt tính làm việc theo chu trình kín và liên tục. Kết quả nghiên cứu thực tế cho biết kích thước hạt than hoạt tính càng nhỏ thì độ ngậm H2S của than càng lớn. Thường người ta sản xuất than có cỡ hạt 1÷2 mm.
Ngoài ra, để quá trình hấp phụ của than hoạt tính xảy ra được triệt để, khí thải cần được lọc sạch bụi để đưa nồng độ bụi xuống còn 2÷3 mg/m3 trước khi đưa vào hệ thống hấp phụ.
Thông tin liên hệ đơn vị có khả năng xử lý khí thải Hydro Sunfua (H2S)
Quý doanh nghiệp hãy liên hệ tới Công ty TNHH Đầu Tư Phát Triển TM XD Thiên Long. Công ty chúng tôi với đội ngũ thạc sĩ, kỹ sư giàu kinh nghiệm đã đầu tư nghiên cứu, đánh giá kỹ lưỡng khi xử lý khí thải Hydro Sunfua (H2S) và tìm các phương án xử lý khí thải Hydro Sunfua (H2S) chất lượng tốt nhất, chi phí hợp lý và thời gian nhanh nhất.
- Với phương châm: “Uy tín, chất lượng là hàng đầu” Thiên Long mang đến cho quý khách hàng sản phẩm và dịch vụ tốt nhất, đáp ứng nhu cầu cần thiết của quý khách.
- Quý khách hàng có công trình, dự án cần tư vấn, hãy gọi ngay qua hotline 0965.565.579 để nhận được sự hỗ trợ nhanh nhất và tận tình nhất.

Bài viết cùng chủ đề:
-
Xử lý mùi từ hệ thống xử lý nước thải
-
Xử lý bụi lò hơi
-
Phương pháp xử lý khí thải lò hơi đốt trấu hiệu quả
-
Phương pháp xử lý khí thải lò đúc gang hiệu quả
-
Giải pháp xử lý mùi nhà máy cao su
-
Công nghệ xử lý khí thải lò hơi đốt hạt điều
-
Hệ thống thông gió trại heo
-
Phương pháp xử lý khí thải lò hơi đốt củi hiệu quả
-
Xử lý bụi sơn hiệu quả đạt chuẩn
-
Xử lý khí thải lò hơi đốt mùn cưa
-
Cách xử lý mùi trại gà hiệu quả
-
Công nghệ xử lý khí thải lò hơi đốt than đá hiệu quả
-
Đơn vị lắp đặt hệ thống xử lý bụi hiệu quả
-
Phương pháp xử lý bụi kim loại hiệu quả
-
Công nghệ xử lý mùi trại heo hiệu quả
-
Hệ thống xử lý khí thải lò nung thép
















